④リコンビナントワクチン(NVX-CoV2373) の副反応
NVX-CoV2373 Phase 3臨床試験で生じた服反応の発生状況を図4に示します。全部で2310人(ワクチン群+プラセボ群)に副反応が認められた(5)。
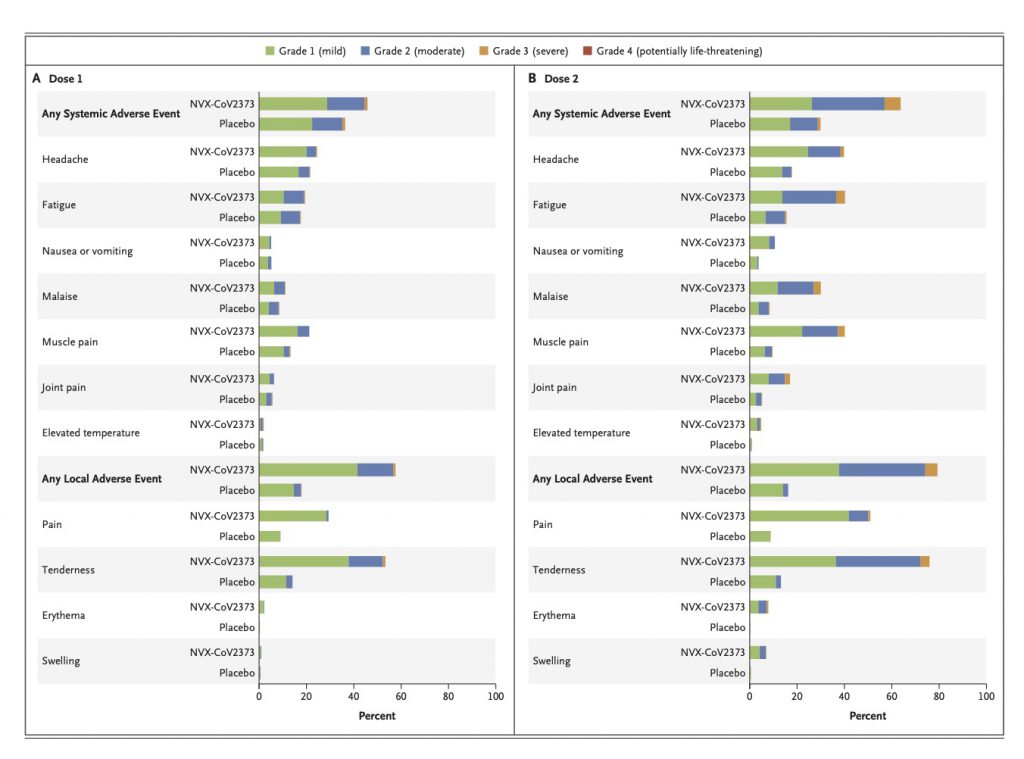
通常生じうる局所反応は、1ドーズ目(ワクチン群57.6%、プラセボ群17.9%)、2ドーズ目(ワクチン群76.4%、プラセボ群51.2%)とワクチン群により高頻度に認められた。大部分は局注部位の圧痛と疼痛で、grade 1(軽度)~grade 2(中等度)レベルであった。1ドーズ目(圧痛53.3%、疼痛29.3%)、2ドーズ目(圧痛76.4%、疼痛51.2%)での3日以内に消失していた。mRNAワクチン同様に64歳以下の若年層に多い傾向であった。
全身反応は1ドーズ目(ワクチン群45.7%、プラセボ群36.3%)、2ドーズ目(ワクチン群64.0%、プラセボ群30.0%)とワクチン群により高頻度に認められた。1ドーズ目で、頭痛(24.5%)、筋痛(21.4%)、全身倦怠感(19.4%)、2ドーズ目で頭痛(40.0%)、筋痛(40.3%)、全身倦怠感(40.3%)でいずれもgrade 1〜2レベルで2日以内に回復している。
grade 4レベルの重篤な副反応はワクチン接種群の3例に認められそのうち2例は40℃を超える熱発であった。残る1例はCOVID-19感染によるもので入院に至った。ワクチン投与群における38℃以上の熱発は1ドーズ目で2.0%、2ドーズ目で4.8%、grade 3レベルの39℃〜40℃の熱発は1ドーズ目で0.4%、2ドーズ目で0.6%であった。想定外の重度の副反応として2ドース完遂後3日目で心筋炎が1例報告されたが2日間の入院で完全回復していた(市中ウイルス感染による心筋炎との鑑別不能)。
[結語]
リコンビナントワクチンの出現により、mRNAワクチンの作用機序から想定される将来的不安の多くは解消されると考えられる。リコンビナントワクチンの効果はmRNAワクチンとほぼ同等と考えられ、副反応が非常にマイルドであることからも若年から高齢者まですべての年齢で接種可能なワクチンとして今後は汎用されるワクチンとなりうると考えられる。しかしながら、ワクチン接種によりADE(VADE)が誘発される可能性は払拭できたわけではないのでコロナウイルスワクチンに関しては、すべての種類のワクチン接種に関して慎重に経過監視を行う必要性があると考えられる。
Uploaded on July 21, 2021.
参考文献
1. Pollet J, Chen WH, et al. Recombinant protein vaccines, a proven approach against coronavirus pandemics. Advanced Drug Delivery Reviews 2021; 170: p71-82
2. Shinde V, Z Bhikha, et al. Efficacy of NVX-CoV2373 Covid-19 Vaccine against the B.1.351 Variant. N Engl J Med 2021;384:1899-1909.
DOI: 10.1056/NEJMoa2103055
3. Reimer JM, Karlsson KH, et al.Matrix-MTM adjuvant induces local recruitment, activation and maturation of central immune cells in absence of antigen. PLoS ONE 2012(7); 7. e41451
4. Keech C, Albert G, et al. Phase 1–2 Trial of a SARS-CoV-2 Recombinant Spike Protein Nanoparticle Vaccine. N Engl J Med 2020;383:p2320-2332.
DOI: 10.1056/NEJMoa2026920
5. Heath PT, Galiza EP, et al. Safety and efficacy of NVX-CoV2373 covid-19 vaccine. N Engl J Med 2021: DOI: 10.1056/NEJMoa2107659