(1) COVID-19ワクチンはコロナウイルスのどの部分に向けて作られているのか?について
COVID-19(SARS-COV2)ウイルス粒子は、図1のAにある様に4つの主要構造を持つ。スパイク蛋白(S: Spike protein)、ヌクレオカプシド蛋白(N: Nucleocapsid protein)、エンベロープ蛋白(E: Envelope protein)、膜蛋白(M: Membrane protein)でありこの各蛋白が免疫源性を持ちワクチンのターゲットになる。このうち中和抗体(Neutralizing antibody)と呼ばれているものは主にスパイク蛋白(以下S蛋白と略す)に対するIgG抗体である(先行して自然収束したSARS-COV1ウイルスの中和抗体の同定、モノクローナル抗体の精製により同じ機序で細胞に感染するSARS-COV2の中和抗体もスパイク蛋白に対する抗体であることがわかっている(1)。
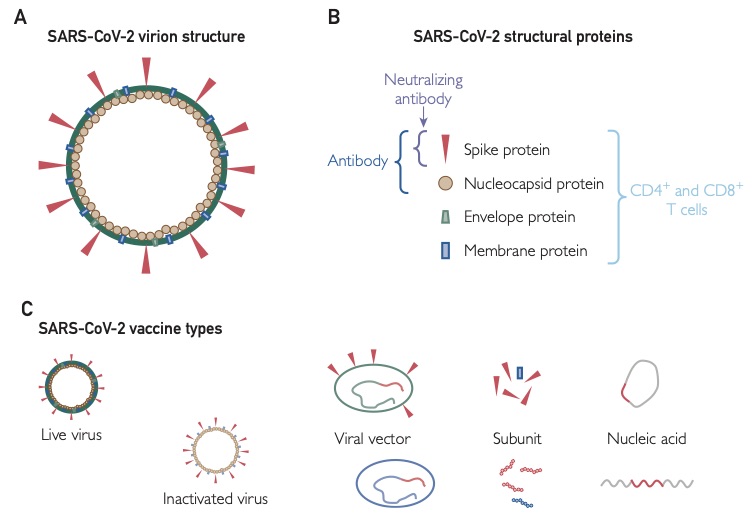
現在ワクチンに関しては世界中で200近い種類の治験が進行していて、生/不活化ワクチン、核酸ワクチン(mRNA/DNA)、ウイルスベクターワクチン、サブユニットワクチンなどがあるが当然ながら現時点で治験が終了して安全性と効果持続性に関して保障されたものは全くない。WHOは、COVID19の猛威を危惧して緊急使用としてmRNAワクチン2種類(ファイザー社のBNT162b1およびb2(商品名コミナティー)とモデルナ社のmRNA-1273)を認可した。これはこの2者が他よりも先行して短期の治験終了の結果を出したからに過ぎない。mRNAワクチンは詳しくは後述するがS蛋白をターゲットにしたワクチンで、主に中和抗体の産生を機序とする感染防御を目論んだワクチンである。
(2)スパイク蛋白とReceptor Binding Domein(RBD)領域について
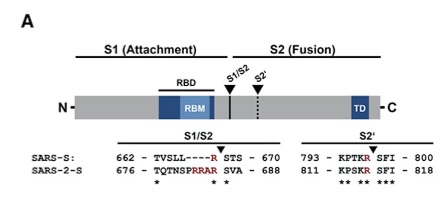
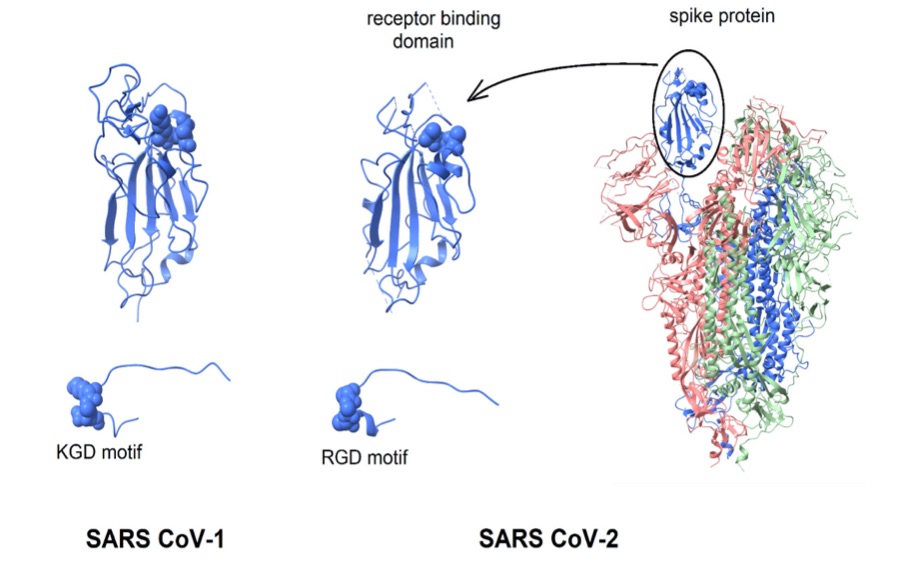
SARS-COV1とSARS-COV2のウイルスRNA塩基配列の〜76%に相同性があり、両者がS蛋白を介して細胞表面にACE2(アンギオテンシン変換酵素2型)受容体を発現している細胞に侵入する感染パターンを共有していることが明らかとなっている。この際セリンプロテアーゼであるTMPRSS2により図2のS1/S2およびS2’部位が切断されることが必要である(2)。S1/S2部位切断をきっかけにSARS COV-2はスパイク蛋白の先端に位置するRBD領域がACE2と融合することで標的細胞に接着する。SARS-COV2はSARS-COV1よりも10倍以上ACE2受容体に親和性が強いことから感染性の大きさが推測できるが、この機序のみではSARS-COV2の強大な感染性を説明するには不十分である。図3に示されたRBD領域に存在するRGDモチーフがターゲットとなる細胞表面のインテグリンと結合することでACE2受容体を発現していない細胞とも結合することが可能となり、症状の重篤化に拍車をかけている可能性がある(3)。