rt-PCR(real time Polymerase Chain Reaction)検査は、全世界的にCOVID19感染症診断のゴールドスタンダードとなっているが、検査の時点で症状がない場合、PCR検査陽性のみでは治療が必要な現在進行中の新規感染者であるのか、回復期にある既感染者であるのかは鑑別不能である。ここで評価基準の参考となるのがCt(Cycle Threshold)値である。
①PCR法におけるCt値について
PCR法で核酸増幅を行う場合、原理的には1回の増幅反応過程でターゲットである検体試料のDNAまたはRNAは2倍量に増加する(100%反応効率が得られた場合)。
したがってt回の反応操作を行った場合の検体試料のPCR産物であるアンプリコンの数をNtとすると、
Nt=2Nt-1=2*2Nt-2=2*3Nt-3=………=2*tNo (Noは検体試料の初期値)
と漸化式から求まる。したがってPCR産物は指数関数的に増加することになるので増幅サイクル数とPCR最終産物の量をあらかじめ測定検証してあるスタンダード検体と比較することで目的検体の初期量が推測可能であろうことは直感的にも理解できるロジックである。
リアルタイムPCR(rt-PCR)法では、蛍光色素を用いて各増幅サイクルごとにPCR産物であるアンプリコンの数(蛍光シグナル)を測定する(1)。蛍光シグナルをサイクル数に対してプロットしていくことでPCRの全反応過程を通して蓄積されるPCR産物のグラフを得ることができるのでrt-PCR法を用いることで検体試料の初期濃度を非常に正確に定量することが可能となる。
rt-PCR法は特定の配列特異的なプライマー(一般的に18〜24ヌクレオチドになるようにデザインされている)を使用して長さが50〜150塩基対となるようなアンプリコンを得ることを目標としている。自明のことではあるが検体試料中にプライマーと相補対となる配列が多く存在する場合は、早い段階(サイクル数)で増幅が確認できる。これは検体採取部位でのウイルス増殖の度合いをそのまま反映していることは容易に想像できる。
rt-PCR法は標準的には、トータル40サイクルで実施される。反応のバックグラウンド(ベースライン)として初期の3〜15サイクルで得られるシグナルレベルが設定され、これ以下のシグナルは全てノイズとみなされる。このベースラインシグナルよりも優位な増加を示すシグナルレベルを閾値(threshold line)といい、通常ベースラインのσ(標準偏差)の10倍値が設定される。この閾値とアンプリコンの蛍光シグナルが交差する時点のサイクル数をCt値(Cycle Threshold)という。Ct値は検体試料の初期量と反比例するのでCt値が小さいほど検体に含まれるウイルス量が多いと評価できる。
Ct値をCOVID19感染症の感染リスクや重症化傾向との関連に言及させるのであれば、まず安定した量のアンプリコンが得られる適切な部位からの目的検体採取を行うことが前提条件となる。これには食事や飲水などによる希釈や洗い流し効果を受けにくい部位からの採取が必要であり、同部位からの同時期複数検体採取でPCR核酸増幅法によリ得られるアンプリコンの量の分散値が小さいとうい条件が必須である。このように確実で安定した検体採取部位及び採取方法として、Torrettaらは下図のような鼻咽頭ぬぐい液と中咽頭ぬぐい液採取の2つを挙げている(2)。
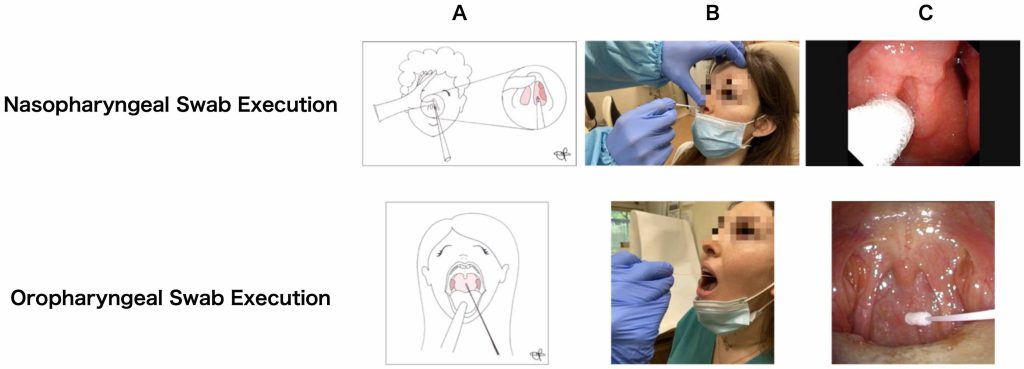
the Literature. Ear, Nose & Throat Journal 2021; 100(2S): pp131S–138SのFigure2, 3より引用
いずれも検査者の暴露リスクを伴う採取法であるのでフルPPEもしくはPCRブースを用いた換気の良い場所での採取が好ましいと考えられる。
*用語について:文中で略語が不明瞭になっていましたので修正しました。
RT-PCR(Reverse Transcription PCR): RNAをPCR法で増幅するために一旦RNA→DNAへ逆転写可能である逆転写酵素(reverse transcriptase)を用いて拡散増幅を行う方法です(RT-PCR=逆転写+PCR拡散増幅)。RT-PCRが汎用の略記です。ウイルスなどのRNAの塩基配列を同定したり、増幅→cDNAクローンニングを行う際に用いられる手法です。
rt-PCR(real time PCR): PCR法に蛍光色素を用いて各サイクルごとのPCR産物を測定する定量的PCR法のことを示します。rt-PCRが汎用の略記となります。正確にはrt-PCR法には、DNA断片をそのまま拡散増幅するrt-PCRとRNAを増幅する逆転写過程が加わったrt-RT-PCRの2つが含まれます。COVID19のrt-PCR検査では,、上述の逆転写によりDNAを合成するステップが加わりますので正確にはrt-RT-PCRを示します。
δ株までは感染成立から発病までの潜伏期(Incubation Period: IP)が5~6日前後と長く、その間に存在する無症状であるが感染性のあるウイルスを排出するため感染伝播を生じる症状発症前感染( Pre-Symptomatic Transmission: PST)を高率に認めるのがCOVID19感染症の特徴であることは既に周知の事実であることは言うまでもない。これは感染成立から感染待ち時間(感染性を獲得するまでの時間)がIPに比して非常に短いことを示しており、感染したのではないかというイベントに直面した場合(いわゆる濃厚接触)、症状がなくても早々に感染媒介者と化してしまうことを意味する。PSTにより感染者本人が発病するまでに周囲に新たな感染者を2~3人前後生み出すと言われていたが、実際には感染者のPCR検査に基づく鼻咽頭のウイルスの保有量はCt値で約15~32前後とまちまち(当クリニックでの経験値)であり、各個体で感染力が異なると考えられる。 理論的には、COVID19の感染力(β)は[飛沫及びエアロゾル粒子1個に含まれる感染性ウイルスの量(C)] x [ 単位時間あたりに発生する粒子数(N)] x [暴露時間(T)]に比例することはCOVID19の主たる感染経路がバイオエアロゾル感染であることを考慮すると直感的に理解できる。比例定数をαとして、β=αCNTと表すと感染力をコントロールする個人的努力要因はエアロゾルの発生量の抑制と暴露時間の短縮(=直面会話の制限)であり、エアロゾル粒子の感染成立浮遊域(直面距離で2m前後)を考えればソーシャルディスタンシングの重要性は言うまでもない。図2に見られるようにCOVID19感染症では、発症直前から直後の時点で保有ウイルス量がピークに達することはもはや常識化しているが、この後のウイルス動態は減少する傾向を辿る。実際の上気道標本からのウイルス培養分離は症状の消失時期である10日前後でほとんど検出できなくなる(3)。しかしながらこの時期でのPCR法で得られるCt値は33前後ある場合が多く、陰性(世界標準でCt値40)となるまでには1ヶ月以上を要す。これに対してよく比較に用いられるインフルエンザウイルス感染症では、症状発症後からウイルスが増殖するため感染対策は、発症後早々にマスク着用と自宅療養を行えばよくウイルス毒性が高い(鳥インフルエンザなど)場合を除き感染対策はかなり行いやすい。実際のところ、常時マスク着用となっているここ2年間でのインフルエンザウイルス感染症の発生件数は極端に減少している。

δ株までのデータでは疾患重症度は異なるものの、おおよそのウイルス動態は一致しているので発症後の入院隔離期間は基本的に10日程度で、付帯条件としてPCR法によるCT値40の達成のオプションが加わっていた、
③COVID19(〜δ株)感染症におけるCt値の経時変化について
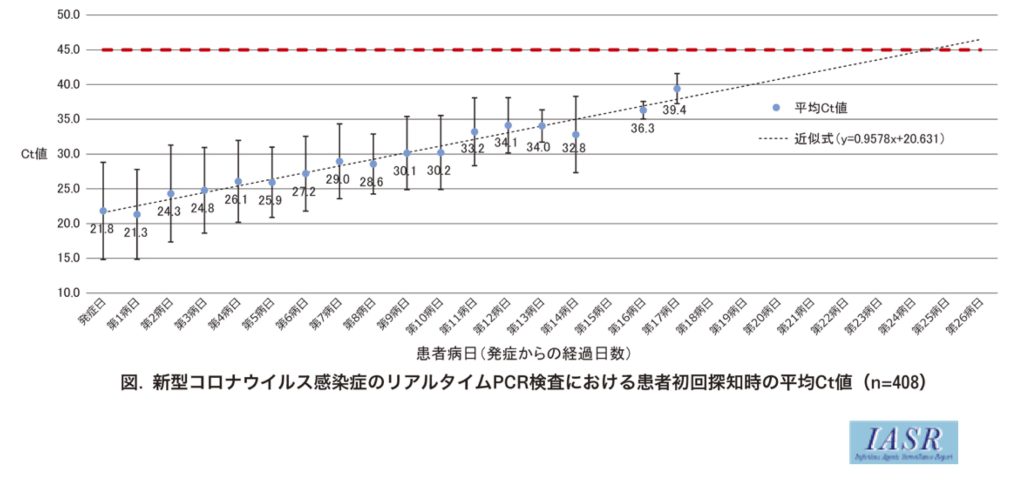
408例の国内COVID19確定診断症例(当時α株相当)に対してRT-PCR法で得られた平均Ct値の経時推移(発症〜第17病日目まで)に関して国立感染研究所が報告しているものがある(4)。Ct値は発症日に最低(ウイルス量が多い)で以後漸増し、各病日の平均Ct値の最小二乗法による線形近似式はy=0.9578x+20.631, 相関係数 は0.9652であったと報告してある(下図3)。発症から14日の時点でもCt値が30未満の症例が存在している。
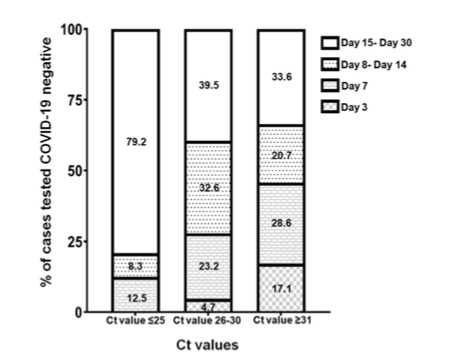
Aranha Cらは、Cobas 6800 を用いて発症日のCt値とその後30日までの間にPCR陰性となるまでに要する日数を比較検討している(5)。Ct値が低い(ウイルス量が多い)ほど陰性化するまでの日数を要すといった直感通り結果が見える。こういった傾向を踏まえると、発症時のCt値により隔離日数の重み付を変更することが可能かもしれない。もちろんそのためには適切な部位から適切な手法で検体が採取されていることが大前提ではある。
前述のごとくPCR検査陽性のみでは、現在進行形の治療が必要な感染者か、放置可能な回復期の感染者かは判別不能である。よって臨床症状の有無とCt値をもって鑑別がなされる。有症状の場合は、判定を疑う余地はほとんどないと考えられるが、無症状経過の場合は上述のようなCt値の経時推移データを熟知した上での慎重な判定が必要である(6)。以上の知識を持ち合わせていても被検者に感染イベントの心当たりがない場合、感染成立初期の立ち上がりの時期と真の無症状患者の回復期の鑑別は困難なのである程度の隔離期間をおいて経過観察する必要がある。非効率的な過程を排除するためには好き勝手にPCR検査を自由化するのはいいことであるとは思えない。この点ウイルスを可視化できるマスクなどがコマーシャルベースに乗れば無駄な検査を減らすのに貢献するであろう。
このようにCt値の経時推移が明らかになってくると今度はCt値がいくらであれば放置しても市中感染を拡大しない症例なのか?という問題に直面することになる。Ct値と感染伝播(感染リスク)に関する論文をPubmedで検索してもわずか数編しかヒットしてこない。 Singanayagam A らは、図5に示すようなCt値とウイルス分離培養陽性率との関係を報告している(7)。概ねウイルス培養分離率が10%以下となるCt値35以上を感染リスクほとんどなしと評価しているようである( Ct値35付近では、長い塩基配列のアンプリコンの形成(=感染性のあるアクティブなウイルス)がほとんど認められず ).
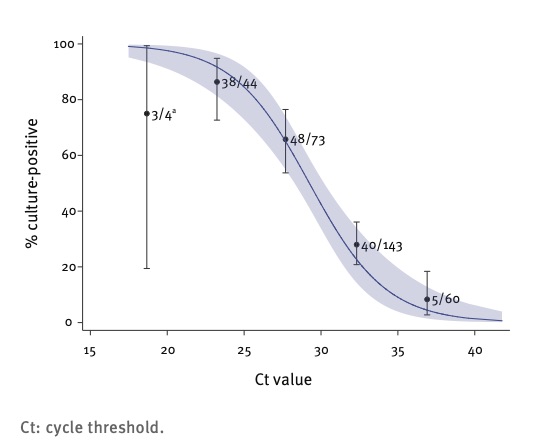
Ct値35の回復期の患者から感染が成立するかどうかは量子論における確率問題に帰するように思える。適切に感染対策が個人で行われていることを前提にCt値をベースに感染リスクを考慮するのであれば、Ct値35は市中感染を拡大しないという基準は妥当なのかもしれない。
一方、迅速抗原定性検査として汎用されているQuickNavi(TM)-COVID19 Agキットに関して、Kiyasuらは、無症候性、有症候性症例に対する感度をそれぞれ67.1% (55.4–77.5)、89.3% (82.0–94.3)と報告している(8)。図6にあるようにCt値が30以上(ウイルス量が少ない)では有症状でも検出率は30%を下回る様子なので抗原定性検査陰性でも疑わしい場合はPCR検査で再評価を行う必要性がある。逆にCOVID19感染を強く疑う症例でも抗原検査陰性であればCt値は30以上である可能性は高いといえるので門前で抗原定性検査を行うことでより院内感染対策に役立つのではないかと考えられる。

オミクロン株に関しては潜伏期が2日前後に短縮している上に、比較的派手な症状で発症する傾向があるのでデルタ株以前よりは公衆衛生対策での効果が出やすいことが予想されるが、不意打ちのごとく海外からの持ち込みによるアウトブレークが生じたため一斉風靡した。現時点では症状経過に基づいた隔離期間が採用されている上にCt値による最終評価はほとんんど行われていない。何を根拠に隔離期間の短縮を決定しているのか判然としないが、隔離明けの時点でCt値が市中感染の拡大や高止まりの原因とならないレベルに到達しているのかどうかは確認すべきではないかと考える。実際のところ発症後1W近く経過して受診した症例で、Ct値が10~20台の高ウイルス状態にある症例を経験している。オミクロン株に関しては、今までの症状経過に基づく隔離期間の設定よりCt値ベースでの隔離期間を短縮/延長を考えるべきなのかもしれない。診断時のCt値によっては隔離の必要性がない場合もあるのかもしれないが現時点でオミクロン株のCt値の経時推移に関しての評価論文はほとんど見当たらない。
ただし、ウイルス1個が体内に侵入した場合、感染が成立するかどうかに関しては感染症学において結論は出ていない。ほぼ無症候性の陽性者の感染拡大リスクは有症状者の約1/2に相当すると見積もられているが(→See Part2)、なぜかはその後解明されていない。無症状陽性者のCt値が平均的に低いのかどうかもはっきりしていない。恐らく真の無症状陽性者は相当まれで、ほとんどは自分の症状に気がついていないか、後に発症しても単なる感冒として処理されていて統計に反映されていないのではと考える。
Uploaded on April 4, 2022.
参考文献
1. リアルタイムPCRハンドブック Thermo Fisher Scientific pp 1-19
2. Torretta S, Zuccotti G, et al. Diagnosis of SARS-CoV-2 by RT-PCR Using Different Sample Sources: Review of
the Literature. Ear, Nose & Throat Journal 2021, Vol. 100(2S) 131S–138S
3. Sethuraman N, Jeremiah SS, et al. Interpreting Diagnostic Tests for SARS-CoV-2. JAMA June 9, 2020 Volume 323, Number 22 2249-2251.
4. 蜂巣友嗣 門倉圭佑(他). 患者病日とリアルタイムPCR Ct値の相関について. IASR 2020(7) Vol. 41 pp 117-118
5. Aranha C, Patel V, et al. Cycle threshold values in RT‐PCR to determine dynamics of SARS‐CoV‐2 viral load: An approach to reduce the isolation period for COVID‐19 patients. J Med Virol. 2021;1–4.
6. Fox-Lewiss A, Fox-Lewiss S, et al. ARS-CoV-2 viral load dynamics and real-time RT-PCR cycle threshold interpretation in symptomatic non- hospitalised individuals in New Zealand: a multicentre cross sectional observational study. Pathology 2021; 53(4): pp 530–535
7. Singanayagam A, Patel M, et al. Duration of infectiousness and correlation with RT-PCR cycle threshold values in cases of COVID-19, England, January to May 2020. Euro Surveill. 2020;25(32):pii=2001483. https://doi.org/10.2807/1560-7917.ES.2020.25.32.2001483
8. Kiyasu Y, Takeuchi Y, et al. Prospective analytical performance evaluation of the QuickNaviTM-COVID19 Ag for asymptomatic individual. Journal of Infection and Chemotherapy 2021; 27: pp 1489–1492
[院長の独り言]
新型コロナウイルス感染症の収束という事象を考えると究極的には統計力学における等分配の法則よりも、むしろパレートの2:8の法則に従うと推定される。これに基づくと最終規模は日本全体で人口の2割に相当する2000万人前後が感染し、その2%に当たる40万人が死亡した時点で収束に至るという推測になる(これは西浦教授が初期に予測した数値に近いが一度のウエーブでこれが生じなかったのは幸いである)。日本がどのような根拠をもってウィズコロナに適応しようとしているのかは不明であるが、少なくともウィズコロナ宣言を始めた英国やUSAは、すでに途方もない感染者数と関連死者数を計上しており2 : 8の法則のに近い状況に到達している。現行mRNAワクチンは結局のところその場しのぎの緊急回避手段にすぎない(これが、FDAの最初の認可基準であり今も変わってはいない)。ただ想定以上に有効期間が短っかかったため頻回接種を推し進めざるを得なくなったということ。人口の20%ほどに存在するこのウイルスに対する脆弱な集団をどうやって防御するかが当初からの課題であったはずであるが、いつの間にか解釈が拡大投影され何人に対しても強力な殺人ウイルスのようなイメージが植え付けられてしまっている。延々とワクチン接種を完了してもウイルスに対して脆弱性を有する集団が延々と繰り返すウェーブで毎回少しずつ削られていくのをもう3年間も見せ付けられてきた。この集団は、罹患してしまうと重症化/死亡のリスクがどうしても高くなる。これらの国々が上記背景を科学的根拠に、これ以上死者は増加しないと確信をもって開放に向かっているのであれば、このような背景を考慮せずウィズコロナに安易に同調するのは無謀であると私は思う。表現は好ましくないが、恐らく感染により持病の悪化等で死亡するであろうと予測される脆弱な集団がほぼ淘汰されつくしつつある欧米とゼロコロナ対策で感染者と死者を究極に抑え込んできた東アジア諸国では事情は大きく異なる。東アジアは今後もしばらく困難な状況がつづくのかもしれない。そのような状況を考慮するとまだしばらく公共施設や人込みではマスク着用は必要であろう。その中には一見健常者に見えてもウイルスに脆弱性を示す集団は必ず混在している。ただ国民が理解しなければならないのは、少なくとも医療機関をはじめ関連する施設、多くの公共施設は常にゼロコロナを目標とせねばならず、訪問者が安心して利用できる聖域である必要がある。持病をかかえるようになればすぐわかることであるが全通院患者にとって新型コロナウイルスは脅威である。こういった施設を利用する際には自己中心的な行動は一切認められないということ。